Page 34 - RECCMI_Diciembre_20
P. 34
Cruz M, Graña-Cruz DC, Pérez L, Gaudiano J. Rituximab en lupus sistémico ampolloso
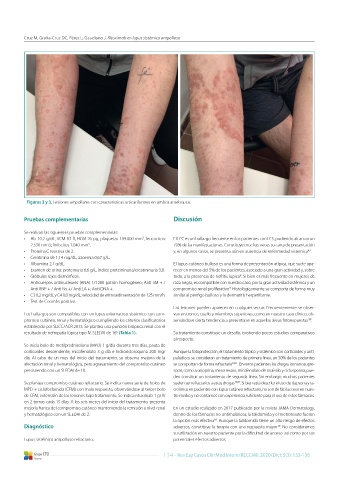
Figuras 2 y 3. Lesiones ampollares con características urticariformes en ambos antebrazos.
Pruebas complementarias Discusión
Se realizan las siguientes pruebas complementarias:
3
• Hb 10,2 g/dL, VCM 83 fl, HCM 26 pg, plaquetas 109.000 mm , leucocitos: El LEC es un hallazgo frecuente en los pacientes con LES, pudiendo alcanzar un
3
2.530 mm3; linfocitos 1.040 mm . 70% de las manifestaciones. Constituye muchas veces su carta de presentación
• Proteína C reactiva de 2. y, en algunos casos, se presenta aún en ausencia de enfermedad sistemica .
6,7
• Creatinina de 1,14 mg/dL, azoemia 0,67 g/L.
• Albumina 2,1 g/dL. El lupus cutáneo bulloso es una forma de presentación atípica, que suele apa-
• Examen de orina: proteinuria 6,6 g/L, índice proteininuria/creatininuria 3,8. recer en menos del 5% de los pacientes, asociado a una gran actividad y, sobre
• Glóbulos rojos dismórficos. todo, a la presencia de nefritis lupica . Si bien es más frecuente en mujeres de
8
• Anticuerpos antinucleares (ANA) 1/1280 patrón homogéneo; Anti SM + / raza negra, es compatible con nuestro caso, por la gran actividad sistémica y un
Anti RNP + / Anti Ro +/ Anti LA +; Anti DNA +. compromiso renal proliferativo . Histológicamente se comporta de forma muy
4
• C3 0,2 mg/dL y C4 0,0 mg/dL; velocidad de eritrosedimentación de 125 mm/h. similar al pénfigo bulloso y la dermatitis herpetiforme.
• Test de Coombs positivo.
Las lesiones pueden aparecer en cualquier sector. Frecuentemente se obser-
Los hallazgos son compatibles con un lupus eritematoso sistémico con com- van en tronco, cuello y miembros superiores, como en nuestro caso clínico, ob-
4,9
promiso cutáneo, renal y hematológico cumpliendo los criterios clasificatorios servándose cierta tendencia a presentarse en aquellas áreas fotoexpuestas .
establecido por SLICC/ACR 2013. Se plantea una punción biópsica renal con el
resultado de nefropatía lúpica tipo IV, SLEDAI de 16 (Tabla 1). Su tratamiento constituye un desafío, existiendo pocos estudios comparativos
5
al respecto.
Se inicia bolo de metilprednisolona (MPD) 1 g/día durante tres días, pauta de
corticoides descendente, micofenolato 3 g día e hidroxicloroquina 200 mg/ Aunque la fotoprotección, el tratamiento tópico y sistémico con corticoides y anti-
día. Al cabo de un mes del inicio del tratamiento, se observa mejoría de la palúdicos se consideran un tratamiento de primera línea, un 50% de los pacientes
afectación renal y hematológica, pero agravamiento del compromiso cutáneo se comportan de forma refractaria 10,11 . En estos pacientes las drogas inmunosupre-
persistiendo con un SLEDAI de 10. soras, como azatioprina, metotrexato, micofenolato de mofetilo y ciclosporina, pue-
den constituir un tratamiento de segunda línea. Sin embargo muchos pacientes
Se plantea compromiso cutáneo refractario. Se indica nueva serie de bolos de suelen ser refractarios a estas drogas 10,11 . Si bien está descrito el uso de dapsona y ta-
MPD + ciclofosfamida (CFM) con mala respuesta, observándose al tercer bolo crolimus en pacientes con lupus cutáneo refractario, no son de fácil acceso en nues-
de CFM, extensión de las lesiones bajo tratamiento. Se indica rituximab 1 gr IV tro medio y no contamos con experiencia suficiente para el uso de estos fármacos.
en 2 tomas cada 15 días. A los seis meses del inicio del tratamiento, presenta
mejoría franca del compromiso cutáneo manteniendo la remisión a nivel renal En un estudio realizado en 2017 publicado por la revista JAMA Dermatology,
y hematológico con un SLEDAI de 2. dentro de los fármacos no-antimaláricos, la talidomida y el metrotexate fueron
10
la opción más efectiva . Aunque la talidomida tiene un alto riesgo de efectos
Diagnóstico adversos, constituye la terapia con una respuesta mayor . No consideramos
10
su utilización en nuestro paciente por la dificultad de acceso así como por sus
Lupus sistémico ampolloso refractario. potenciales efectos adversos.
134 Rev Esp Casos Clin Med Intern (RECCMI). 2020 (Dic); 5(3): 133-136